保健食品批文转让流程
保健食品批文转让(即技术转让)需遵循严格的法规流程,主要分为合同公证、样品试制与检测、材料申报、技术审评及行政审批五个阶段。以下是综合最新规定的完整流程及关键注意事项:

一、转让流程
1. 签订转让合同
• 转让方与受让方明确转让价格、权利义务、违约责任等条款,需经公证处公证。
2. 试制样品与检测
• 受让方在转让方指导下生产3批中试样品;
• 完成稳定性试验及卫生学、功效成分检测报告。
3. 准备申报材料
• 包括:公证合同、原批准证书、受让方资质文件、产品配方工艺、质量标准、标签说明书样稿、3批样品检测报告等。
4. 提交申请与受理
• 向国家市场监督管理总局食品审评中心提交材料,5个工作日内确认受理。
5. 技术审评与现场核查
• 技术审评:评估安全性、功能有效性及工艺一致性等;
• 现场核查:检查受让方生产条件是否符合原市场工艺环境要求。
6. 审批与颁证
• 综合审评上报→ 行政审批→ 注销原批文,颁发新证书。
总周期约12-20个月,受材料完整性、审评进度影响。
二、核心注意事项
1. 受让方资质要求
• 需具备保健食品生产许可证,相应剂型生产线通过认证(可委托有资质企业生产)。
2. 合同风险防范
• 需约定“转让失败的责任归属”,技术审评不审核合同内容,双方需自行承担注册失败风险。
3. “双无”产品谨慎转让
• 无有效期、无技术要求的老批文(如2003年前批准),可能存在配方或工艺不合规风险,需提前评估。
4. 名称变更限制
• 产品名称变更需提交命名说明,且不得与现有药品或保健食品重名。
5. 禁用原料核查
• 配方含朱砂、雄黄、八角莲等59种禁用物质(见卫生部禁用名单)的批文无法转让。
三、所需关键材料清单
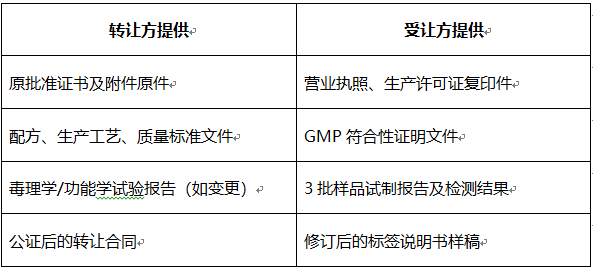
提示:进口批文转让还需提供生产国官方公证文件及驻华使领馆确认。
四、常见问题解答
• Q:批文转让期间原证书是否有效?
→ 需确保在证书有效期内完成转让,否则需申请延续注册。
• Q:多个持有人如何转让?
→ 需所有持有人联合签署转让合同。
• Q:转让失败能否退款?
→ 取决于合同约定,建议明确“技术审评不通过”的退费条款。
建议委托专业代理机构(如小蓝中康等)规避流程风险。完整法规参考《保健食品注册与备案管理办法》。
(更多细节可参考国家市场监督管理总局官网或咨询专业机构之一 如:小蓝中康)
小蓝中康(北京)科技有限公司-保健食品研发领域领先技术服务商,为您提供保健食品研发·保健食品注册·保健食品备案·保健食品转让·保健食品延续·保健食品变更的管家式服务。
注:以上内容均由AI搜集总结并生成,仅供参考。若您期望获取专业服务,请致电400-070-1617进行咨询。
点击进入~获取专属方案,服务热线:400-070-1617、13261985261(微信同号)












